肺腺癌是肺癌的一种,属于非小细胞肺癌,占肺癌总数的35%-50%。肺腺癌具有较强的转移能力,是导致癌症患者死亡的主要原因之一。胆固醇是一种主要的脂质物质,是细胞膜和细胞器膜的基本成分,胆固醇对于癌症发展过程中介导活性膜运输和信号转导至关重要。与乳腺或肝脏等富含脂肪、富含胆固醇的器官相比,肺部的胆固醇含量较低,而胆固醇是如何在肺腺癌中积累,且胆固醇是如何影响肺腺癌的发展及其内在机制尚不清楚。FOXA3作为直接调控的转录因子,以及脂肪组织和肝脏中脂质和葡萄糖代谢的关键调控因子,有报道称FOXA3在肺腺癌中高表达,FOXA3在气道上皮细胞中过表达可能增加与病毒感染相关的慢性肺部疾病。然而,FOXA3是否参与了肺腺癌转移中的脂质代谢有待进一步研究。
2024年5月28日,华东师范大学徐凌燕教授团队在 PLoS Biology 在线发表题为 FOXA3 regulates cholesterol metabolism to compensate for low uptake during the progression of lung adenocarcinoma 的研究论文,本研究证明在肺腺癌中外源性胆固醇作为信号分子,通过GLI2-FOXA3-HMGCS1信号通路,诱导内源性胆固醇生物合成,导致膜组成的改变和癌细胞迁移,揭示了胆固醇代谢和FOXA3对肺腺癌转移的独特作用。
研究团队使用伯桢生物的生长因子Recombinant Human R-spondin1(861-RS1)、Recombinant Human Noggin( 807-NOG)、Recombinant Human FGF7(923-FG7)、Recombinant Human FGF10(816-FGF)、细胞活性(ATP)检测试剂盒Organoid Viability ATP Assay Kit(E238003)及类器官冻存液Organoid Cryopreservation Medium(Serum Free)(E238023) ,成功构建了正常气管类器官和非小细胞肺癌类器官并完成了全篇类器官实验。基于类器官模型,作者发现FOXA3和HMGCS1在肿瘤中表达更高,当用FOXA3抑制剂magnolol处理高表达FOXA3和HMGCS1的肿瘤类器官时,magnolol可有效抑制肿瘤类器官中与细胞转移相关基因的表达,且效果优于传统的化疗药物氟伐他汀和顺铂。在本研究中,类器官作为个性化癌症治疗模型在机制验证和药效检测方面发挥了重要作用。
外源性胆固醇促进肺腺癌细胞内源性胆固醇生物合成以及癌细胞迁移
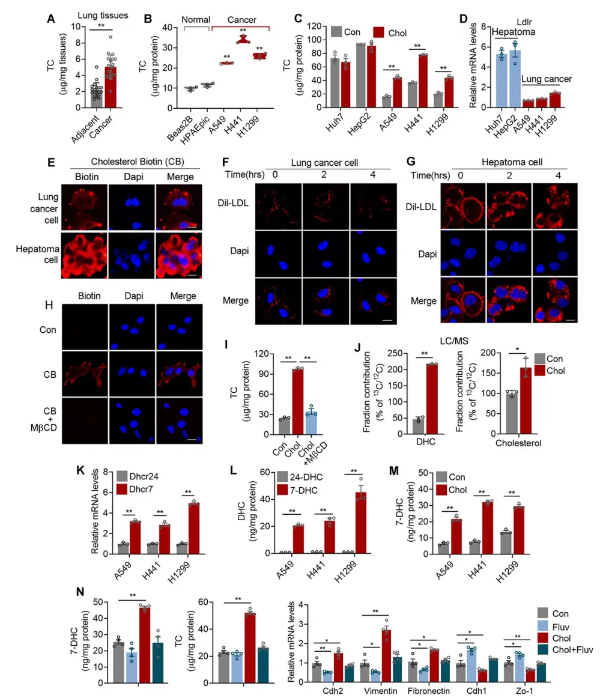
作者使用胆固醇对肺癌和肝癌细胞系进行处理,结果显示通过外源性胆固醇处理后肝癌细胞内的胆固醇水平不再增加甚至受到轻微抑制,而肺癌细胞内的胆固醇水平得到显著提高。与此同时,在mRNA和蛋白水平上肺癌细胞被证明具有更强的迁移能力。作者进一步用生物素标记的胆固醇(CB)处理肺腺癌细胞,观察到CB主要保留在肺腺癌细胞的细胞膜上,而在肝癌细胞中大量CB被内化到细胞质中。与肝癌细胞相比,肺腺癌细胞中胆固醇受体LDL受体(LDLR)的表达显然更低,且带有荧光的LDL(Dil-LDL)仍保留在肺癌细胞的细胞膜上,而Dil-LDL明显以时间依赖的方式被吸收到肝癌细胞质中。随后作者用甲基-β-环糊精(MβCD)对肺癌细胞的膜信号转导进行干扰,发现给予CB不再与膜结合,并未能增加肺腺癌细胞的胆固醇水平。接下来的13 C示踪表明,外源性胆固醇能有效地激活肺腺癌患者内源性胆固醇从头合成,13 C-脱氢胆固醇(DHC)和13 C-胆固醇含量显著增加。有趣的是,作者发现DHCR7的mRNA水平显著高于DHCR24,胆固醇处理显著提高了肺癌细胞中的7-DHC水平。氟伐他汀是一种可以抑制胆固醇生物合成的物质,结果显示氟伐他汀处理可抑制外源性胆固醇诱导的肺癌细胞内7-DHC和胆固醇水平的升高,以及抑制转移相关基因的表达。综上所述,外源性胆固醇通过有效激活肺腺癌中内源性胆固醇从头合成、诱导7-DHC以及胆固醇水平升高来促进癌细胞迁移。(图1)
图1 肺腺癌细胞感知外源性胆固醇信号通过从头生物合成获得胆固醇并用于细胞迁移
FOXA3是介导肺腺癌细胞中外源性胆固醇诱导的内源性胆固醇生物合成的关键转录因子
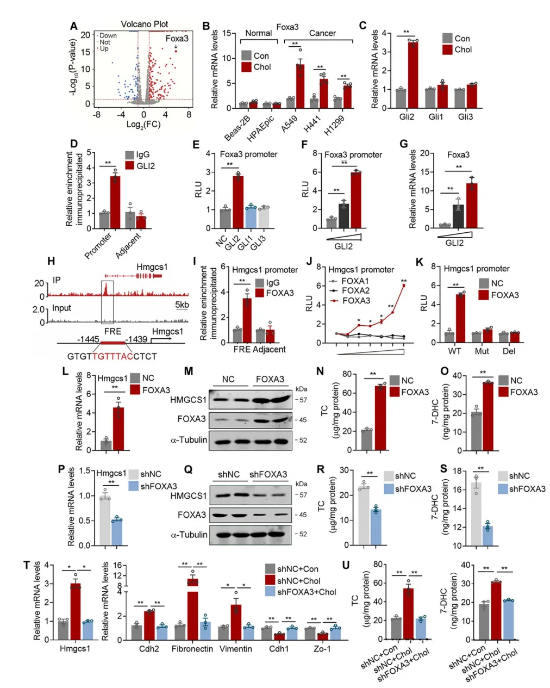
作者对胆固醇处理组和对照组细胞进行转录组分析,结果显示存在34个差异表达的转录因子,其中脂质代谢中的关键转录因子FOXA3排名第一。经qPCR验证,胆固醇处理后肺腺癌细胞中FOXA3 mRNA水平显著上调。并且,在转录组分析中,作者发现hedgehog信号通路下游信号分子GLI2的表达水平增加,进一步数据表明胆固醇处理可特异性诱导GLI2的表达。随后通过ChIP实验、荧光素酶检测和qPCR分析表明,外源性胆固醇通过GLI2诱导了肺腺癌细胞中FOXA3的转录。接下来,通过RNA-seq数据集与ChIP-seq数据集的重叠分析发现,HMGCS1是作为FOXA3直接靶基因的首选候选基因之一,且在胆固醇处理后表达水平显著增加。随后通过ChIP实验和荧光素酶检测证实,FOXA3促进了HMGCS1的转录,而HMGCS1启动子上推测的FOXA3结合位点的缺失或突变导致了HMGCS1无法转录。而FOXA3表达下调降低了肺癌细胞中HMGCS1的表达、细胞胆固醇水平和7-DHC水平。重要的是,根据作者之前的数据,外源性胆固醇处理增加了细胞胆固醇水平和7-DHC水平,并增强了肺腺癌细胞中FOXA3、HMGCS1和转移相关基因的表达,而这些影响在FOXA3基因敲除的情况下被消除。综上所述,FOXA3可能是外源性胆固醇通过GLI2-FOXA3-HMGCS1轴诱导的内源性胆固醇生物合成和进展的关键转录因子。(图2)
图2 FOXA3是介导肺腺癌细胞中胆固醇诱导的内源性胆固醇生物合成的关键转录因子
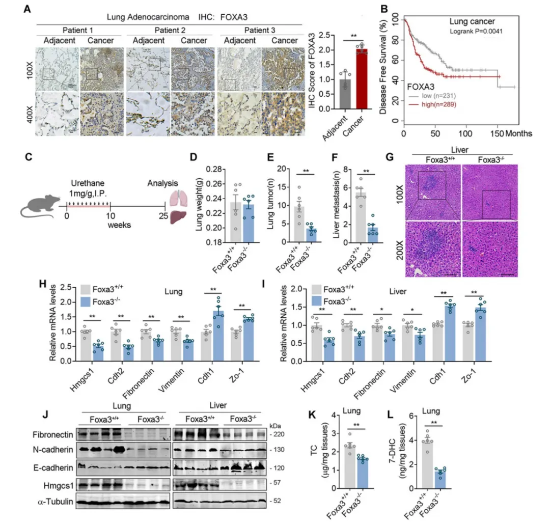
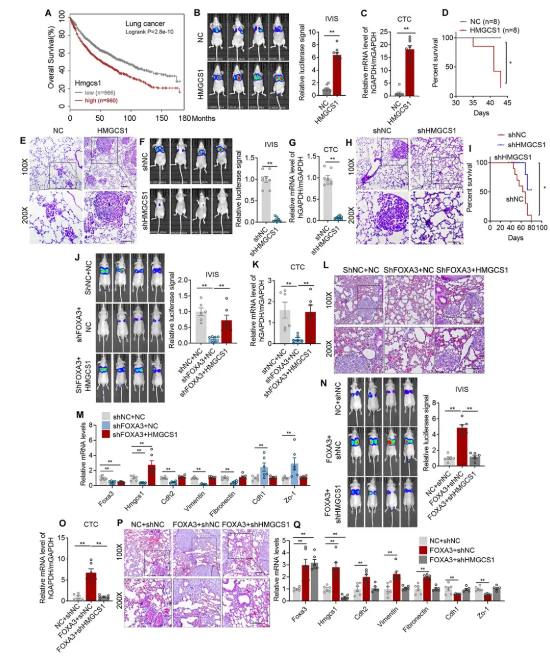
作者通过qPCR、Western blot和免疫组化等手段证实,与邻近组织相比,肿瘤组织中FOXA3水平有明显增强。此外,癌症基因组图谱(TCGA)数据库的Kaplan-Meier绘图仪表明高FOXA3水平与不良预后相关。为了证明FOXA3在肺腺癌转移中的作用,作者通过氨基甲酸乙酯(一种化学性肺致癌物)处理WT和FOXA3-/- 小鼠。结果显示,与WT小鼠相比,FOXA3-/- 小鼠的肺重量无显著差异,而肺部肿瘤淋巴结的数量显著减少,并且肺癌向肝脏的转移明显减少,同时肺部和肝脏中HMGCS1表达和转移标志物显著降低,肺部中胆固醇和7-DHC水平受到抑制。(图3)
图3 FOXA3 -/- 小鼠模型中的肺癌细胞转移
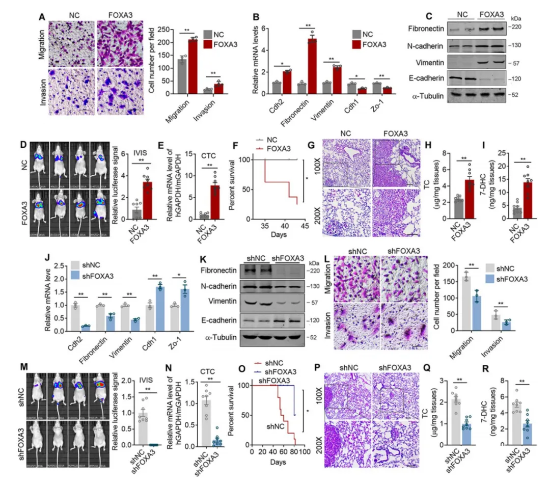
接下来作者对肺腺癌细胞中FOXA3进行过表达(FOXA3-OE)处理,CCK8及细胞迁移实验结果表明FOXA3-OE显著增强了细胞迁移和侵袭能力。同时,作者使用荧光素酶标记的FOXA3-OE肺癌细胞对小鼠尾静脉进行注射,结果显示,与对照组相比,FOXA3-OE细胞的荧光素酶信号增强,循环肿瘤细胞(CTC)增加,小鼠生存率更低,肺部转移区域增加,胆固醇和7-DHC水平升高,并且肺组织中HMGCS1和EMT的标记物水平也显著升高,证明FOXA3-OE可以提高肺腺癌细胞体内迁移能力。为了进一步证实FOXA3在肿瘤转移中的作用,作者建立了FOXA3-OE小鼠肺癌细胞LLC的皮下植入模型,结果显示,过表达FOXA3促进了肺部转移和随后的皮下LLC肿瘤的生长。与此同时,作者构建了FOXA3敲低(FOXA3-KD)细胞,FOXA3-KD细胞在体内和体外均表现出与FOXA3-OE相反的表型,如荧光素酶信号减弱,小鼠存活率增加,胆固醇水平和7-DHC水平降低等。综上所述,FOXA3促进了肺癌细胞的转移。(图4)
图4 FOXA3在体内外均能促进肺癌细胞的转移
HMGCS1促进肺癌细胞迁移,是FOXA3的下游效应物
除了FOXA3,癌症基因组图谱(TCGA)数据库的Kaplan-Meier绘图仪表明,GLI2和HMGCS1表达水平高与肺癌患者总生存率降低呈正相关,再一次证实GLI2- FOXA3-HMGCS1轴在肺癌转移中的重要作用。事实上,作者发现在肺腺癌细胞中,HMGCS1过表达(HMGCS1-OE)在体外和体内均促进了肺癌细胞的迁移,HMGCS1基因敲除(HMGCS1-KD)则表型相反。此外,作者发现在小鼠中敲除FOXA3抑制了肺部转移,而过表达HMGCS1挽救了这种现象。与此同时,过表达FOXA3在体内外促进了癌细胞迁移,而下调HMGCS1显著消除了这些作用。综上所述,HMGCS1是FOXA3在内源性胆固醇生物合成和肺腺癌进展中的下游效应因子。(图5)
图5 HMGCS1作为FOXA3的下游效应物在体内外均能促进肺癌细胞转移
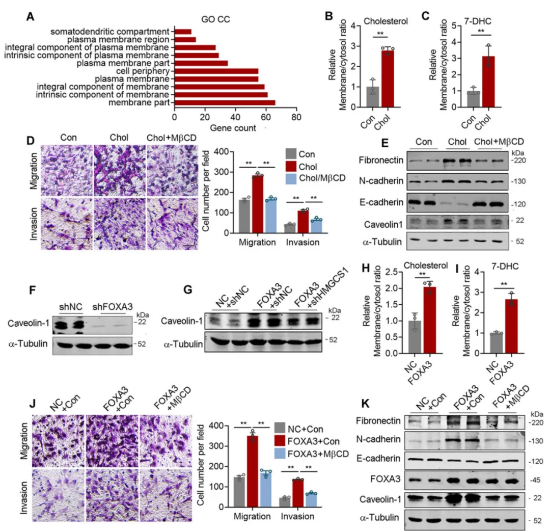
作者为了深入了解肺腺癌细胞中内源性胆固醇水平升高带来的影响,进行了转录组分析,分析表明细胞膜受外源性胆固醇处理后影响最大。事实上,作者发现与肺腺癌细胞的细胞质相比,外源性胆固醇处理后显著增加了胆固醇和7-DHC并入细胞膜,导致膜组成的改变。并且,在肺腺癌细胞中使用外源性胆固醇会导致癌细胞迁移和侵袭增强,转移标志物的表达增加,Caveolin-1表达量增加。但是这些作用均被MβCD处理所消除,因为MβCD破坏了膜信号转导。作者进一步发现,FOXA3-KD降低了Caveolin-1水平,FOXA3-OE增加了Caveolin-1水平,而这种效果可被HMGCS1下调所阻断。并且,与细胞质相比,肺癌细胞中的FOXA3-OE显著增加了胆固醇和7-DHC并入细胞膜,并增强了细胞迁移和转移标志物的表达。综上所述,膜组成的改变部分地参与了肺腺癌细胞中FOXA3-HMGCS1轴诱导的内源性胆固醇生物合成和癌细胞的转移。(图6)
图6 胆固醇诱导细胞膜组成的改变从而促进肺腺癌细胞的迁移
Magnolol抑制FOXA3转录,阻断了患者来源肺腺癌类器官转移相关基因的表达
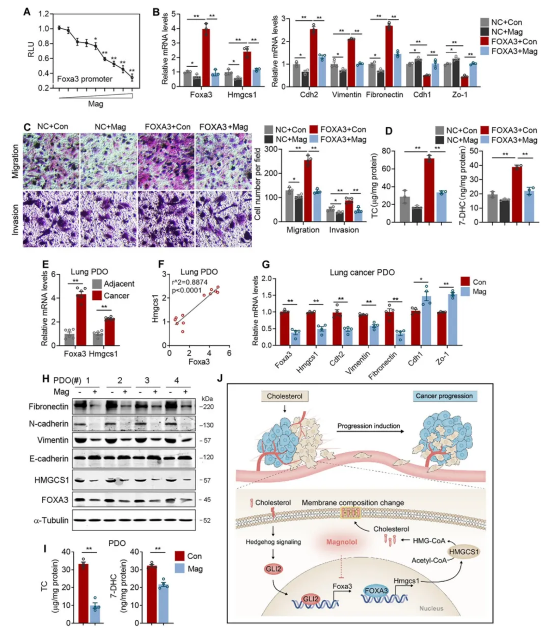
最后作者研究FOXA3的阻断是否会抑制肺腺癌转移,通过FOXA3转录报告基因筛选,鉴定出magnolol,它可有效抑制FOXA3的表达。在肺腺癌细胞中,作者证实了magnolol治疗有效地阻断了FOXA3-OE引起的HMGCS1以及转移相关基因的表达、细胞迁移/侵袭和内源性胆固醇从头合成。进一步结果表明magnolol以剂量依赖的方式特异性抑制FOXA3的表达,并且在没有FOXA3的情况下,magnolol处理对HMGCS1和EMT的表达没有额外的抑制作用。随后作者从患者体内获取肺腺癌及邻近组织构建类器官(PDOs),与之前结果一致,与邻近PDO相比,肿瘤PDO中的FOXA3和HMGCS1表达水平更高。此外,PDO样本中HMGCS1水平与FOXA3水平呈正相关。随后作者选择了4个FOXA3和HMGCS1表达量最高的样本,并对其进行magnolol处理,结果发现magnolol可以有效抑制PDO样本中胆固醇和7-DHC水平,以及抑制转移相关基因在mRNA和蛋白质水平上的表达。该结果表明magnolol可作为一个有效化合物预防肺腺癌的发展,特别是在具有高FOXA3和高HMGCS1表达特征癌症的个性化治疗中。作者发现与氟伐他汀和顺铂相比,magnolol对细胞活力和增殖基因的影响较轻,而对HMGCS1基因表达和细胞转移程序的抑制作用较强。此外,作者还利用裸鼠建立了异种移植模型,植入人A549非小细胞肺癌(NSCLC)细胞,用magnolol或对照组进行治疗。结果表明,magnolol对肺腺癌转移有明显的抑制作用,具有临床转化潜力。综上所述,本研究证明肺腺癌细胞对外源性胆固醇具有独特的正反馈机制,通过激活GLI2-FOXA3-HMGCS1轴增强内源性胆固醇生物合成和细胞胆固醇增加,最终部分地通过膜组成的改变促进肺腺癌发展,而FOXA3抑制剂magnolol可阻断这种信号级联,防止癌症转移。(图7)
图7 Magnolol可作为抗PDOs肺腺癌进展的有效化合物
本研究揭示了肺腺癌中胆固醇代谢的正反馈机制,并确定FOXA3作为感知胆固醇和hedgehog信号通路的关键因子,FOXA3通过HMGCS1促进7-DHC水平升高和内源性胆固醇生物合成,导致膜组成改变以促进癌细胞转移。此外,本研究还利用magnolol作为有效化合物,靶向FOXA3,抑制胆固醇代谢,为治疗肺腺癌转移提供可能性。